Autor:
Roger Morrison
Data Utworzenia:
3 Wrzesień 2021
Data Aktualizacji:
21 Czerwiec 2024

Zawartość
Częścią pracy i nauki radzenia sobie z układem okresowym jest umiejętność określenia, ile protonów, neutronów i elektronów trafia do atomu. W tym artykule dowiesz się, jak to zrobić!
Do kroku
 Znajdź zdjęcie układu okresowego pierwiastków. To jest przegląd wszystkich pierwiastków chemicznych w kolejności (rosnącej) liczby atomowej. Możesz także wyodrębnić inne ważne informacje o pierwiastku, takie jak skrót i masa atomowa. Pozycja w tabeli wskazuje również na inne istotne właściwości elementu.
Znajdź zdjęcie układu okresowego pierwiastków. To jest przegląd wszystkich pierwiastków chemicznych w kolejności (rosnącej) liczby atomowej. Możesz także wyodrębnić inne ważne informacje o pierwiastku, takie jak skrót i masa atomowa. Pozycja w tabeli wskazuje również na inne istotne właściwości elementu. 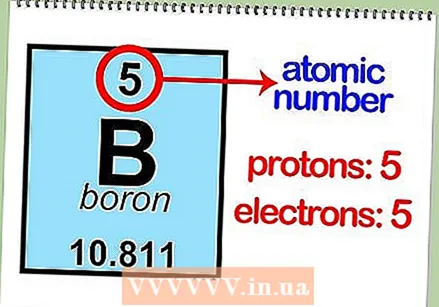 Przeczytaj liczbę atomową pierwiastka. Pozwala to określić liczbę protonów i elektronów. Liczba atomowa znajduje się nad symbolem elementu w ramce. Na przykład bor (B) ma liczbę atomową 5, co oznacza, że ma 5 protonów i 5 elektronów.
Przeczytaj liczbę atomową pierwiastka. Pozwala to określić liczbę protonów i elektronów. Liczba atomowa znajduje się nad symbolem elementu w ramce. Na przykład bor (B) ma liczbę atomową 5, co oznacza, że ma 5 protonów i 5 elektronów. 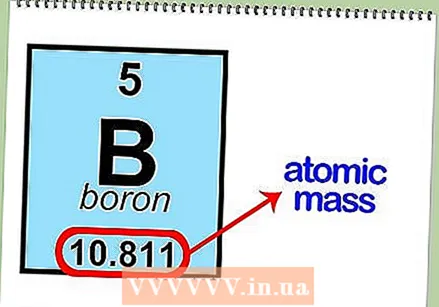 Określ masę atomową pierwiastka. Zwykle można znaleźć tę liczbę pod symbolem atomu. Masa atomowa boru wynosi 10811.
Określ masę atomową pierwiastka. Zwykle można znaleźć tę liczbę pod symbolem atomu. Masa atomowa boru wynosi 10811. 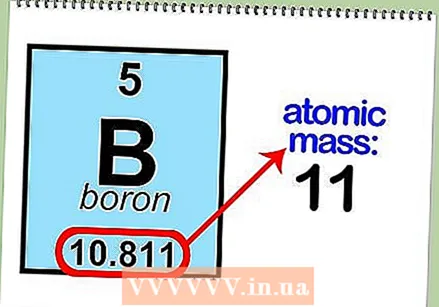 Zaokrąglij masę atomową do najbliższej liczby całkowitej, aby znaleźć masę atomową. Na przykład zaokrąglona masa atomowa boru wynosi 11.
Zaokrąglij masę atomową do najbliższej liczby całkowitej, aby znaleźć masę atomową. Na przykład zaokrąglona masa atomowa boru wynosi 11. 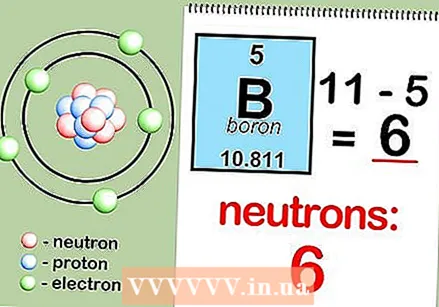 Odejmij liczbę atomową od masy atomowej. Ponieważ większość masy atomowej zależy od protonów i neutronów, odejmując liczbę protonów (liczbę atomową) od masy atomowej, można obliczyć liczbę neutronów w atomie. Na przykład: 11 (masa atomowa) - 5 (liczba protonów) = 6 (liczba neutronów).
Odejmij liczbę atomową od masy atomowej. Ponieważ większość masy atomowej zależy od protonów i neutronów, odejmując liczbę protonów (liczbę atomową) od masy atomowej, można obliczyć liczbę neutronów w atomie. Na przykład: 11 (masa atomowa) - 5 (liczba protonów) = 6 (liczba neutronów). - Zapamiętaj formułę. Aby znaleźć liczbę neutronów w atomie w przyszłości, wystarczy zapamiętać wzór liczba neutronów = masa atomowa - liczba atomowa.