Autor:
Lewis Jackson
Data Utworzenia:
5 Móc 2021
Data Aktualizacji:
1 Lipiec 2024

Zawartość
Mol to standardowa jednostka miary w chemii, używana do badania różnych pierwiastków w związku. Zwykle masę związku oblicza się w gramach (g) i należy ją przeliczyć na jednostki molowe. Przejście jest dość proste, jednak nadal pozostaje kilka ważnych kroków, które musimy wykonać. Korzystając z poniższej metody, możesz łatwo zamienić gramy na mole.
Kroki
Część 1 z 2: Oblicz masę cząsteczkową
Przygotuj niezbędne materiały, aby rozwiązać problem matematyczny. Gdy będziesz mieć wszystkie dostępne narzędzia, łatwiej będzie rozwiązać problem. Potrzebujesz:
- Ołówek i papier. Matematyka staje się łatwiejsza, gdy wszystko zapisujesz na papierze. Musisz przedstawić wszystkie kroki, aby osiągnąć maksymalny wynik.
- Układ okresowy pierwiastków chemicznych: służy do określania masowych atomów pierwiastków.
- Kalkulator kieszonkowy: służy do obliczania skomplikowanych liczb.

Określ, które pierwiastki są w związku, który chcesz zamienić na jednostki molowe. Pierwszym krokiem do obliczenia masy cząsteczkowej jest określenie pierwiastków, z których składa się związek. Jest to łatwe, ponieważ skrót elementów składa się z jednego do dwóch znaków.- Jeśli substancja jest skracana dwoma literami, pierwsza litera będzie wielka, a druga mała. Przykład: Mg to skrót od pierwiastka magnezu.
- Związki NaHCO3 składa się z czterech pierwiastków: sodu (Na), wodoru (H), węgla (C) i tlenu (O).
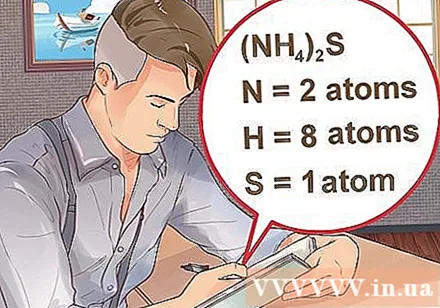
Określ liczbę atomów dla każdego pierwiastka w związku. Musisz znać liczbę atomową każdej substancji w związku, aby obliczyć masę cząsteczki tego związku. Mała liczba obok skrótu elementu oznacza liczbę atomową elementu.- Przykład: związek H.2O ma dwa atomy wodoru i jeden atom tlenu.
- Jeśli związek jest zapisany w nawiasach, któremu towarzyszy mały indeks, każdy składnik w nawiasie mnoży indeks. Przykład: związek (NH4)2S składa się z dwóch atomów N, ośmiu atomów H i jednego atomu S.

Zapisz sześcienny papier atomowy dla każdego pierwiastka. Najprostszym sposobem znalezienia sześciennego atomu pierwiastka jest użycie układu okresowego. Po zlokalizowaniu pierwiastka w układzie okresowym zobaczysz masę atomową tuż pod ikoną pierwiastka.- Na przykład sześcienny atom tlenu wynosi 15,99.
Oblicz masę cząsteczkową. Masa cząsteczki substancji jest równa liczbie atomów każdego pierwiastka pomnożonej przez masowy atom tego pierwiastka. Ta ilość jest niezbędna w przeliczeniu na gram na mol.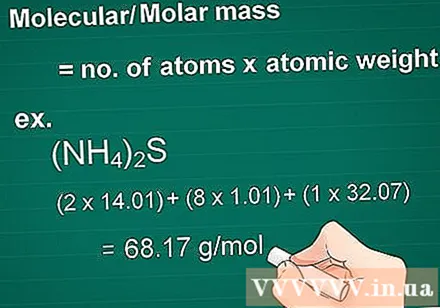
- Najpierw pomnóż liczbę atomową każdego pierwiastka w związku przez jego masowy atom.
- Następnie dodaj razem masy pierwiastków w mieszance.
- Przykład: masa cząsteczkowa związku (NH4)2S = (2 x 14,01) + (8 x 1,01) + (1 x 32,07) = 68,17 g / mol.
- Masa cząsteczkowa jest również znana jako masa molowa.
Część 2 z 2: Zamień gramy na mol
Skonfiguruj formułę konwersji. Aby znaleźć liczbę moli związku, podziel liczbę gramów związku przez masę molową tego związku.
- Wzór: liczba moli = masa (gramy) / masa molowa związku (gram / mol)
Zastąp liczby w formule. Po skonfigurowaniu odpowiedniej formuły następnym krokiem jest zastąpienie obliczonych liczb formułą. Jeśli chcesz się upewnić, że dane są we właściwej pozycji, możesz to sprawdzić, wyłączając jednostkę. Jeśli po prostocie pozostałą jednostką są krety, to jesteś poprawnie ustawiony.
Rozwiązać równanie. Za pomocą kalkulatora podziel masę przez sześcienną cząsteczkę substancji lub związku. Ilorazem będzie liczba moli substancji lub związku, którego szukasz.
- Na przykład problem dotyczy 2 g wody (H.2O) i poproś o przeliczenie go na jednostki molowe. Mamy masę molową H.2O wynosi 18 g / mol. Podziel 2 przez 18, więc masz 0,1111 mol H2O.
Rada
- Nie zapomnij dołączyć nazwy elementu lub związku do odpowiedzi.
- Jeśli zostaniesz poproszony o przedstawienie ćwiczenia lub quizu, upewnij się, że jasno przedstawiłeś odpowiedzi, zakreślając je kółkiem lub rysując ramkę.
Czego potrzebujesz
- Chemiczny układ okresowy pierwiastków
- Ołówek
- Papier
- Komputer
- Problemy chemiczne