Autor:
Marcus Baldwin
Data Utworzenia:
20 Czerwiec 2021
Data Aktualizacji:
13 Móc 2024

Zawartość
- Kroki
- Metoda 1 z 5: Dobre nawyki uczenia się
- Metoda 2 z 5: Zrozumienie struktury atomowej
- Metoda 3 z 5: Obliczanie reakcji chemicznych
- Metoda 4 z 5: Obliczenia
- Metoda 5 z 5: Język chemii
- Porady
Aby zdać egzamin z chemii ogólnej, ważne jest, aby znać podstawy przedmiotu, umieć liczyć, używać kalkulatora do bardziej złożonych problemów i być gotowym na nauczenie się czegoś nowego. Chemia bada substancje i ich właściwości. Wszystko wokół nas dotyczy chemii, nawet najprostsze rzeczy, które uważamy za oczywiste, takie jak woda, którą pijemy i powietrze, którym oddychamy. Przygotuj się na odkrycia dotyczące wszystkiego, co Cię otacza. Poznawanie chemii będzie zabawne.
Kroki
Metoda 1 z 5: Dobre nawyki uczenia się
 1 Poznaj swojego nauczyciela lub nauczyciela. Aby pomyślnie zdać egzamin, powinieneś poznać swojego instruktora i powiedzieć mu, co jest dla Ciebie trudne.
1 Poznaj swojego nauczyciela lub nauczyciela. Aby pomyślnie zdać egzamin, powinieneś poznać swojego instruktora i powiedzieć mu, co jest dla Ciebie trudne. - Do wielu nauczycieli można zwrócić się poza klasą, jeśli uczniowie potrzebują pomocy. Ponadto zwykle posiadają publikacje metodyczne.
 2 Zbierz grupę, aby ćwiczyć. Nie wstydź się, że chemia jest dla Ciebie trudna. Ten temat jest trudny dla prawie wszystkich.
2 Zbierz grupę, aby ćwiczyć. Nie wstydź się, że chemia jest dla Ciebie trudna. Ten temat jest trudny dla prawie wszystkich. - Pracując w grupie, ludzie, którzy potrafią szybko zrozumieć temat, wyjaśnią go innym. Dziel i rządź.
 3 Przeczytaj odpowiednie akapity w samouczku. Podręczniki do chemii nie są najbardziej ekscytującą lekturą, ale powinieneś uważnie przeczytać materiał i podkreślić tekst, którego nie rozumiesz. Zrób listę pytań i pojęć, które są dla ciebie trudne do zrozumienia.
3 Przeczytaj odpowiednie akapity w samouczku. Podręczniki do chemii nie są najbardziej ekscytującą lekturą, ale powinieneś uważnie przeczytać materiał i podkreślić tekst, którego nie rozumiesz. Zrób listę pytań i pojęć, które są dla ciebie trudne do zrozumienia. - Wróć do tych części później z nową głową. Jeśli nadal sprawia Ci to trudność, omów temat w grupie lub poproś o pomoc swojego nauczyciela.
 4 Odpowiedz na pytania po akapicie. Nawet jeśli jest dużo materiału, być może zapamiętałeś więcej, niż myślisz. Spróbuj odpowiedzieć na pytania na końcu rozdziału.
4 Odpowiedz na pytania po akapicie. Nawet jeśli jest dużo materiału, być może zapamiętałeś więcej, niż myślisz. Spróbuj odpowiedzieć na pytania na końcu rozdziału. - Czasami podręczniki mają na końcu materiał wyjaśniający, który opisuje prawidłowe rozwiązanie. Pomoże ci to zrozumieć, gdzie popełniłeś błąd w rozumowaniu.
 5 Przeglądaj wykresy, obrazy i tabele. Podręczniki wykorzystują wizualne środki przekazywania informacji.
5 Przeglądaj wykresy, obrazy i tabele. Podręczniki wykorzystują wizualne środki przekazywania informacji. - Spójrz na zdjęcia i diagramy. Pozwoli to lepiej zrozumieć niektóre pojęcia.
 6 Poproś swojego instruktora o pozwolenie na nagranie wykładu na magnetofonie. Trudno zapisywać informacje i nadal patrzeć na tablicę, zwłaszcza jeśli chodzi o tak złożony temat jak chemia.
6 Poproś swojego instruktora o pozwolenie na nagranie wykładu na magnetofonie. Trudno zapisywać informacje i nadal patrzeć na tablicę, zwłaszcza jeśli chodzi o tak złożony temat jak chemia.  7 Sprawdź poprzednie pytania egzaminacyjne. Czasami uczniowie otrzymują pytania, które napotkali na egzaminach w poprzednich latach, aby mogli lepiej się przygotować.
7 Sprawdź poprzednie pytania egzaminacyjne. Czasami uczniowie otrzymują pytania, które napotkali na egzaminach w poprzednich latach, aby mogli lepiej się przygotować. - Nie zapamiętuj odpowiedzi. Chemia to przedmiot, w którym, aby odpowiedzieć na pytanie, ważne jest, aby zrozumieć, o co chodzi, a nie tylko powtarzać zapamiętany tekst.
 8 Skorzystaj z zasobów edukacyjnych online. Odwiedź wszystkie witryny polecane przez instruktora.
8 Skorzystaj z zasobów edukacyjnych online. Odwiedź wszystkie witryny polecane przez instruktora.
Metoda 2 z 5: Zrozumienie struktury atomowej
 1 Zacznij od najprostszego budynku. Aby zostać egzaminem, musisz wiedzieć, z czego wszystko jest zrobione, co jest treścią i ma masę.
1 Zacznij od najprostszego budynku. Aby zostać egzaminem, musisz wiedzieć, z czego wszystko jest zrobione, co jest treścią i ma masę. - Wszystko zaczyna się od zrozumienia budowy atomu. Cała reszta zostanie dodana z góry. Ważne jest, aby bardzo dokładnie przestudiować wszystkie informacje o atomie.
 2 Sprawdź koncepcję atomu. Atom to najmniejsza „cegła” ze wszystkiego, co ma masę, w tym substancji, których nie zawsze możemy zobaczyć (na przykład gazów). Ale nawet atom zawiera maleńkie cząsteczki, które tworzą jego strukturę…
2 Sprawdź koncepcję atomu. Atom to najmniejsza „cegła” ze wszystkiego, co ma masę, w tym substancji, których nie zawsze możemy zobaczyć (na przykład gazów). Ale nawet atom zawiera maleńkie cząsteczki, które tworzą jego strukturę… - Atom składa się z trzech części - neutronów, protonów i elektronów. Centrum atomu nazywa się jądrem. Jądro składa się z neutronów i protonów. Elektrony to cząstki, które krążą wokół zewnętrznej powłoki atomu, podobnie jak planety wokół Słońca.
- Atom jest bardzo mały. Wyobraź sobie największy stadion, jaki znasz. Jeśli stadion jest atomem, to jądro tego atomu jest wielkości ziarnka grochu.
 3 Dowiedz się, jaka jest struktura atomowa pierwiastka. Pierwiastek jest substancją w naturze, której nie można rozłożyć na mniejsze substancje. Pierwiastki składają się z atomów.
3 Dowiedz się, jaka jest struktura atomowa pierwiastka. Pierwiastek jest substancją w naturze, której nie można rozłożyć na mniejsze substancje. Pierwiastki składają się z atomów. - Atomy w elemencie się nie zmieniają. Oznacza to, że każdy pierwiastek ma w swojej strukturze atomowej pewną unikalną liczbę neutronów i protonów.
 4 Dowiedz się, jak działa jądro. Neutrony w jądrze mają ładunek neutralny. Protony mają ładunek dodatni. Liczba atomowa pierwiastka jest równa liczbie protonów w jądrze..
4 Dowiedz się, jak działa jądro. Neutrony w jądrze mają ładunek neutralny. Protony mają ładunek dodatni. Liczba atomowa pierwiastka jest równa liczbie protonów w jądrze.. - Nie ma potrzeby liczenia liczby protonów w jądrze. Liczba ta jest wskazana w układzie okresowym pierwiastków chemicznych dla każdego pierwiastka.
 5 Policz liczbę neutronów w jądrze. Możesz użyć liczby z układu okresowego. Liczba atomowa pierwiastka jest taka sama jak liczba protonów w jądrze.
5 Policz liczbę neutronów w jądrze. Możesz użyć liczby z układu okresowego. Liczba atomowa pierwiastka jest taka sama jak liczba protonów w jądrze. - Masa atomowa jest wskazana na dole kwadratu każdego pierwiastka pod jego nazwą.
- Pamiętaj, że w jądrze atomu są tylko protony i neutrony. W układzie okresowym podana jest liczba protonów i wartość masy atomowej.
- Teraz wszystko będzie łatwe do obliczenia. Odejmij liczbę protonów od masy atomowej, a otrzymasz liczbę neutronów w jądrze każdego atomu pierwiastka.
 6 Policz liczbę elektronów. Pamiętaj, że przyciągają się cząstki o przeciwnych ładunkach. Elektrony są naładowane dodatnio i krążą wokół atomu. Liczba ujemnie naładowanych elektronów przyciąganych do jądra zależy od liczby dodatnio naładowanych protonów w jądrze.
6 Policz liczbę elektronów. Pamiętaj, że przyciągają się cząstki o przeciwnych ładunkach. Elektrony są naładowane dodatnio i krążą wokół atomu. Liczba ujemnie naładowanych elektronów przyciąganych do jądra zależy od liczby dodatnio naładowanych protonów w jądrze. - Ponieważ sam atom ma ładunek obojętny, liczba cząstek o ładunku ujemnym musi być równa liczbie cząstek o ładunku dodatnim. Z tego powodu liczba elektronów jest równa liczbie protonów.
 7 Zapoznaj się z okresowym układem pierwiastków. Jeśli właściwości pierwiastków są dla ciebie trudne, przestudiuj wszystkie dostępne informacje o układzie okresowym.
7 Zapoznaj się z okresowym układem pierwiastków. Jeśli właściwości pierwiastków są dla ciebie trudne, przestudiuj wszystkie dostępne informacje o układzie okresowym. - Zrozumienie układu okresowego pierwiastków jest niezbędne do pomyślnego zdania egzaminu.
- Układ okresowy składa się wyłącznie z pierwiastków. Każdy element ma symbol alfabetyczny, ten symbol zawsze oznacza ten element. Na przykład Na zawsze oznacza sód. Pełna nazwa elementu znajduje się pod symbolem litery.
- Liczba nad symbolem litery jest liczbą atomową. Jest równa liczbie protonów w jądrze.
- Liczba pod symbolem litery to masa atomowa. Pamiętaj, że masa atomowa to suma protonów i neutronów w jądrze.
 8 Naucz się czytać arkusz kalkulacyjny. W tabeli jest bardzo dużo informacji, od kolorów kolumn po rozmieszczenie elementów od lewej do prawej i od góry do dołu.
8 Naucz się czytać arkusz kalkulacyjny. W tabeli jest bardzo dużo informacji, od kolorów kolumn po rozmieszczenie elementów od lewej do prawej i od góry do dołu.
Metoda 3 z 5: Obliczanie reakcji chemicznych
 1 Napisz równanie. Na zajęciach z chemii nauczysz się określać, co stanie się z elementami po ich połączeniu. Na papierze nazywa się to rozwiązywaniem równania.
1 Napisz równanie. Na zajęciach z chemii nauczysz się określać, co stanie się z elementami po ich połączeniu. Na papierze nazywa się to rozwiązywaniem równania. - Równanie chemiczne składa się z substancji po lewej stronie, strzałki i produktu reakcji. Substancje po jednej stronie równania muszą równoważyć substancje po drugiej stronie.
- Na przykład substancja 1 + substancja 2 → produkt 1 + produkt 2.
- Weź cynę (Sn) w postaci utlenionej (SnO2) i połącz z wodorem w postaci gazu (H2). SnO2 + H2 → Sn + H2O.
- To równanie musi być zrównoważone, ponieważ ilość substancji odczynników musi być równa ilości otrzymanych produktów. Po lewej stronie jest więcej atomów tlenu niż po prawej.
- Zastąp dwie jednostki wodoru po lewej i dwie cząsteczki wody po prawej stronie. W ostatecznej wersji zbilansowane równanie wygląda tak: SnO2 + 2 H2 → Sn + 2 H2O.
 2 Pomyśl o równaniach w nowy sposób. Jeśli trudno jest zrównoważyć równania, wyobraź sobie, że jest to przepis, ale wymaga dostosowania po obu stronach.
2 Pomyśl o równaniach w nowy sposób. Jeśli trudno jest zrównoważyć równania, wyobraź sobie, że jest to przepis, ale wymaga dostosowania po obu stronach. - W zadaniu podajesz składniki po lewej stronie, ale nie mówi, ile musisz wziąć. Równanie mówi również, co się stanie, ale nie mówi, ile. Musisz się dowiedzieć.
- Korzystając z poprzedniego równania jako przykładu, SnO2 + H2 → Sn + H2O, zastanówmy się, dlaczego ten wzór nie zadziała. Ilość Sn jest po obu stronach równa, podobnie jak ilość H2, ale po lewej stronie znajdują się dwie części tlenu, a po prawej tylko jedna.
- Konieczna jest zmiana prawej strony równania tak, aby otrzymany produkt zawierał dwie części H2O. Dwójka przed H2O oznacza, że wszystkie ilości zostaną podwojone. Tlen jest teraz zrównoważony, ale 2 oznacza, że po prawej jest teraz więcej wodoru niż po lewej. Wróć na lewą stronę i podwój wodór, umieszczając przed nim dwa.
- Wszystko jest teraz w równowadze. Ilości wejściowe są równe ilościom wyjściowym.
 3 Dodaj więcej szczegółów do równania. Na zajęciach z chemii zapoznasz się z symbolami oznaczającymi stan fizyczny pierwiastków: t – ciało stałe, g – gaz, w – ciecz.
3 Dodaj więcej szczegółów do równania. Na zajęciach z chemii zapoznasz się z symbolami oznaczającymi stan fizyczny pierwiastków: t – ciało stałe, g – gaz, w – ciecz.  4 Naucz się identyfikować zmiany, które zachodzą podczas reakcji chemicznej. Reakcje chemiczne zaczynają się od podstawowych pierwiastków lub związków, które reagują. W wyniku połączenia otrzymuje się produkt reakcji lub kilka produktów.
4 Naucz się identyfikować zmiany, które zachodzą podczas reakcji chemicznej. Reakcje chemiczne zaczynają się od podstawowych pierwiastków lub związków, które reagują. W wyniku połączenia otrzymuje się produkt reakcji lub kilka produktów. - Aby zdać egzamin, musisz wiedzieć, jak rozwiązywać równania zawierające reagenty lub produkty złożone, lub jedno i drugie.
 5 Poznaj różne rodzaje reakcji. Reakcje chemiczne mogą zachodzić pod wpływem różnych czynników, a nie tylko przy połączeniu pierwiastków.
5 Poznaj różne rodzaje reakcji. Reakcje chemiczne mogą zachodzić pod wpływem różnych czynników, a nie tylko przy połączeniu pierwiastków. - Najczęstsze typy reakcji to synteza, analiza, substytucja, podwójny rozkład, reakcja kwasów i zasad, utlenianie-redukcja, spalanie, izomeryzacja, hydroliza.
- W klasie można badać różne reakcje – wszystko zależy od celów kursu.Na uczelni stopień pogłębienia materiału będzie różnił się od szkolnego programu nauczania.
 6 Wykorzystaj wszystkie dostępne zasoby. Musisz zrozumieć różnicę między podstawowymi reakcjami. Wykorzystaj każdy możliwy materiał, aby zrozumieć tę różnicę. Nie bój się zadawać pytań.
6 Wykorzystaj wszystkie dostępne zasoby. Musisz zrozumieć różnicę między podstawowymi reakcjami. Wykorzystaj każdy możliwy materiał, aby zrozumieć tę różnicę. Nie bój się zadawać pytań. - Nie jest tak łatwo zrozumieć, co zmienia się podczas reakcji chemicznych. To będzie jedno z najtrudniejszych zadań na twoich zajęciach z chemii.
 7 Pomyśl o reakcjach w kategoriach logicznych. Staraj się nie mylić terminologii i komplikuj sprawy jeszcze bardziej. Wszystkie reakcje mają na celu przekształcenie czegoś w coś innego.
7 Pomyśl o reakcjach w kategoriach logicznych. Staraj się nie mylić terminologii i komplikuj sprawy jeszcze bardziej. Wszystkie reakcje mają na celu przekształcenie czegoś w coś innego. - Na przykład już wiesz, co się stanie, jeśli połączysz dwa atomy wodoru i jeden atom tlenu - wodę. Dlatego jeśli wlejesz wodę do rondla i podpalisz, coś się zmieni. Przeprowadziłeś reakcję chemiczną. Jeśli włożysz wodę do lodówki, nastąpi reakcja. Zmieniłeś coś, co dotyczyło reagenta, którym jest woda.
- Przechodź przez każdy rodzaj reakcji, aż wszystko zrozumiesz. Skoncentruj się na źródle energii, które wyzwala reakcję i na głównych zmianach wynikających z reakcji.
- Jeśli trudno ci to zrozumieć, zrób listę niezrozumiałych niuansów i pokaż ją swojemu nauczycielowi, kolegom uczniom lub każdemu, kto jest dobrze zorientowany w chemii.
Metoda 4 z 5: Obliczenia
 1 Poznaj kolejność podstawowych obliczeń. W chemii czasami potrzebne są bardzo dokładne obliczenia, ale często wystarczy podstawowa znajomość matematyki. Ważne jest, aby zrozumieć, w jakiej kolejności przeprowadzane są obliczenia.
1 Poznaj kolejność podstawowych obliczeń. W chemii czasami potrzebne są bardzo dokładne obliczenia, ale często wystarczy podstawowa znajomość matematyki. Ważne jest, aby zrozumieć, w jakiej kolejności przeprowadzane są obliczenia. - Najpierw obliczenia wykonuje się w nawiasach, potem obliczenia w potęgach, potem mnożenie lub dzielenie, a na końcu dodawanie lub odejmowanie.
- W przykładzie 3 + 2 x 6 = ___, poprawna odpowiedź to 15.
 2 Nie bój się zaokrąglać bardzo długich liczb. W chemii często się zaokrąglają, ponieważ często odpowiedzią na równanie jest liczba z dużą liczbą cyfr. Jeśli w opisie problemu znajdują się instrukcje dotyczące zaokrąglania, weź je pod uwagę.
2 Nie bój się zaokrąglać bardzo długich liczb. W chemii często się zaokrąglają, ponieważ często odpowiedzią na równanie jest liczba z dużą liczbą cyfr. Jeśli w opisie problemu znajdują się instrukcje dotyczące zaokrąglania, weź je pod uwagę. - Wiesz, jak zaokrąglać. Jeśli następna cyfra wynosi 4 lub mniej, należy ją zaokrąglić w dół, jeśli 5 lub więcej niż 5, należy ją zaokrąglić w górę. Na przykład tutaj jest numer 6.66666666666666. Zadanie mówi o zaokrągleniu odpowiedzi do drugiej cyfry po kropce. Odpowiedź to 6,67.
 3 Zrozum, czym jest wartość bezwzględna. W chemii niektóre liczby mają znaczenie absolutne, a nie matematyczne. Wartość bezwzględna to wszystkie wartości do liczby od zera.
3 Zrozum, czym jest wartość bezwzględna. W chemii niektóre liczby mają znaczenie absolutne, a nie matematyczne. Wartość bezwzględna to wszystkie wartości do liczby od zera. - Innymi słowy, nie masz już wartości ujemnych i dodatnich, tylko odległość do zera. Na przykład wartość bezwzględna -20 to 20.
 4 Poznaj wszystkie popularne jednostki miary. Oto kilka przykładów.
4 Poznaj wszystkie popularne jednostki miary. Oto kilka przykładów. - Ilość substancji mierzy się w molach (mol).
- Temperatura jest mierzona w stopniach Fahrenheita (° F), Kelvina (° K) lub Celsjusza (° C).
- Masę mierzy się w gramach (g), kilogramach (kg) lub miligramach (mg).
- Objętość cieczy mierzy się w litrach (l) lub mililitrach (ml).
 5 Ćwicz tłumaczenie wartości z jednego systemu pomiarowego na drugi. Na egzaminie będziesz miał do czynienia z takimi tłumaczeniami. Być może trzeba będzie przeliczyć temperaturę z jednego systemu na inny, funty na kilogramy, uncje na litry.
5 Ćwicz tłumaczenie wartości z jednego systemu pomiarowego na drugi. Na egzaminie będziesz miał do czynienia z takimi tłumaczeniami. Być może trzeba będzie przeliczyć temperaturę z jednego systemu na inny, funty na kilogramy, uncje na litry. - Możesz zostać poproszony o udzielenie odpowiedzi w jednostkach innych niż jednostki w opisie problemu. Na przykład w tekście zadania temperatura zostanie wskazana w stopniach Celsjusza, a odpowiedź będzie potrzebna w stopniach Kelvina.
- Zwykle temperaturę reakcji chemicznych mierzy się w stopniach Kelvina. Ćwicz konwertowanie stopni Celsjusza na Fahrenheita lub Kelvina.
 6 Nie spiesz się. Przeczytaj uważnie tekst problemu i naucz się przeliczać jednostki miary.
6 Nie spiesz się. Przeczytaj uważnie tekst problemu i naucz się przeliczać jednostki miary.  7 Wiesz, jak obliczyć stężenie. Doskonal swoją wiedzę z podstaw matematyki, obliczając wartości procentowe, proporcje i proporcje.
7 Wiesz, jak obliczyć stężenie. Doskonal swoją wiedzę z podstaw matematyki, obliczając wartości procentowe, proporcje i proporcje.  8 Poćwicz z danymi żywieniowymi na opakowaniu. Aby zaliczyć chemię, musisz umieć obliczyć proporcje, proporcje i procenty w różnych sekwencjach.Jeśli jest to dla Ciebie trudne, rozpocznij szkolenie w znanych jednostkach miary (na przykład na opakowaniach żywności).
8 Poćwicz z danymi żywieniowymi na opakowaniu. Aby zaliczyć chemię, musisz umieć obliczyć proporcje, proporcje i procenty w różnych sekwencjach.Jeśli jest to dla Ciebie trudne, rozpocznij szkolenie w znanych jednostkach miary (na przykład na opakowaniach żywności). - Weź pakiet danych żywieniowych. Zobaczysz obliczenie kalorii na porcję, zalecaną porcję dziennie jako procent, całkowitą zawartość tłuszczu, procent kalorii z tłuszczu, całkowitą ilość węglowodanów oraz podział według rodzaju węglowodanów. Naucz się obliczać różne wskaźniki na podstawie tych wartości.
- Na przykład oblicz ilość tłuszczów jednonienasyconych w tłuszczu ogółem. Konwersja na procent. Oblicz liczbę kalorii w paczce, znając liczbę porcji i zawartość kalorii w każdej porcji. Oblicz, ile sodu znajduje się w połowie opakowania.
- Pomoże to łatwo przetłumaczyć wartości chemiczne z jednego systemu na inny, na przykład mole na litr, gramy na mol i tak dalej.
 9 Naucz się używać numeru Avogadro. Ta liczba odzwierciedla liczbę cząsteczek, atomów lub cząstek w jednym molu. Stała Avogadro to 6,022x1023.
9 Naucz się używać numeru Avogadro. Ta liczba odzwierciedla liczbę cząsteczek, atomów lub cząstek w jednym molu. Stała Avogadro to 6,022x1023. - Na przykład, ile atomów znajduje się w 0,450 molach Fe? Odpowiedź: 0,450 x 6,022 x 1023.
 10 Pomyśl o marchewkach. Jeśli trudno Ci zrozumieć, jak używać liczby Avogadro, spróbuj policzyć marchewki, a nie atomy, cząsteczki lub cząsteczki. Ile marchewek jest w tuzinie? Wiemy, że tuzin to 12, co oznacza, że w jednym tuzinie jest 12 marchewek.
10 Pomyśl o marchewkach. Jeśli trudno Ci zrozumieć, jak używać liczby Avogadro, spróbuj policzyć marchewki, a nie atomy, cząsteczki lub cząsteczki. Ile marchewek jest w tuzinie? Wiemy, że tuzin to 12, co oznacza, że w jednym tuzinie jest 12 marchewek. - Odpowiedzmy teraz na pytanie, ile marchewek jest w krecie. Zamiast mnożyć przez 12, mnożymy przez liczbę Avogadro. W krecie znajduje się 6,022 x 1023 marchewek.
- Liczba Avogadro służy do zamiany dowolnej wartości atomów, cząsteczek, cząsteczek lub marchewki na mole.
- Jeśli znasz liczbę moli substancji, to wartość liczby cząsteczek, atomów lub cząstek będzie równa tej liczbie pomnożonej przez liczbę Avogadro.
- Zrozumienie, w jaki sposób cząsteczki są przekształcane w mole, jest ważnym czynnikiem podczas egzaminu. Konwersje moli są częścią obliczeń proporcji i proporcji. Oznacza to ilość czegoś w pieprzykach jako część czegoś innego.
 11 Zrozum molarność. Pomyśl o liczbie moli substancji w cieczy. Bardzo ważne jest zrozumienie tego przykładu, ponieważ mówimy o molarności, czyli proporcji substancji wyrażonej w molach na litr.
11 Zrozum molarność. Pomyśl o liczbie moli substancji w cieczy. Bardzo ważne jest zrozumienie tego przykładu, ponieważ mówimy o molarności, czyli proporcji substancji wyrażonej w molach na litr. - Molarność lub stężenie molowe to termin wyrażający ilość substancji w cieczy, to znaczy ilość substancji rozpuszczonej w roztworze. Aby uzyskać molarność, musisz podzielić mole substancji rozpuszczonej na litry roztworu. Molarność wyraża się w molach na litr.
- Oblicz gęstość. Gęstość jest często stosowana w chemii. Gęstość to masa substancji chemicznej na jednostkę objętości. Zazwyczaj gęstość wyraża się w gramach na mililitr lub gramach na centymetr sześcienny - to to samo.
 12 Zredukuj równania do wzoru empirycznego. Oznacza to, że odpowiedź będzie poprawna tylko wtedy, gdy wszystkie wartości sprowadzisz do najprostszej postaci.
12 Zredukuj równania do wzoru empirycznego. Oznacza to, że odpowiedź będzie poprawna tylko wtedy, gdy wszystkie wartości sprowadzisz do najprostszej postaci. - Nie dotyczy to wzorów cząsteczkowych, ponieważ wskazują one dokładne proporcje pierwiastków chemicznych tworzących cząsteczkę.
 13 Dowiedz się, co zawiera wzór cząsteczkowy. Formuły cząsteczkowej nie trzeba sprowadzać do najprostszej czy empirycznej postaci, ponieważ mówi ona, z czego dokładnie zbudowana jest cząsteczka.
13 Dowiedz się, co zawiera wzór cząsteczkowy. Formuły cząsteczkowej nie trzeba sprowadzać do najprostszej czy empirycznej postaci, ponieważ mówi ona, z czego dokładnie zbudowana jest cząsteczka. - Wzór cząsteczkowy jest napisany przy użyciu skrótów pierwiastków i liczby atomów każdego pierwiastka w cząsteczce.
- Na przykład wzór cząsteczkowy wody to H2O. Oznacza to, że każda cząsteczka wody zawiera dwa atomy wodoru i jeden atom tlenu. Wzór cząsteczkowy acetaminofenu to C8H9NO2. Każdy związek chemiczny ma wzór cząsteczkowy.
 14 Pamiętaj, że matematyka w chemii nazywa się stechiometrią. Natkniesz się na ten termin. To jest opis tego, jak chemia jest wyrażana we wzorach matematycznych. W matematyce chemicznej lub stechiometrii ilości pierwiastków i związków chemicznych są często wyrażane w molach, procentach w molach, molach na litr lub molach na kilogram.
14 Pamiętaj, że matematyka w chemii nazywa się stechiometrią. Natkniesz się na ten termin. To jest opis tego, jak chemia jest wyrażana we wzorach matematycznych. W matematyce chemicznej lub stechiometrii ilości pierwiastków i związków chemicznych są często wyrażane w molach, procentach w molach, molach na litr lub molach na kilogram. - Będziesz musiał przekonwertować gramy na mole.Masa atomowa jednostki pierwiastka w gramach jest równa jednemu molowi tej substancji. Na przykład masa atomowa wapnia wynosi 40 jednostek masy atomowej. Tak więc 40 gramów wapnia to jeden mol wapnia.
 15 Poproś o dodatkowe zadania. Jeśli równania i konwersje są dla ciebie trudne, porozmawiaj ze swoim nauczycielem. Poproś o więcej zadań, abyś mógł sam nad nimi pracować, dopóki nie zrozumiesz istoty wszystkich zjawisk.
15 Poproś o dodatkowe zadania. Jeśli równania i konwersje są dla ciebie trudne, porozmawiaj ze swoim nauczycielem. Poproś o więcej zadań, abyś mógł sam nad nimi pracować, dopóki nie zrozumiesz istoty wszystkich zjawisk.
Metoda 5 z 5: Język chemii
 1 Naucz się rozumieć wykresy Lewisa. Wykresy Lewisa są czasami nazywane wykresami punktowymi. Są to proste diagramy, na których kropki reprezentują wolne i związane elektrony w zewnętrznej powłoce atomu.
1 Naucz się rozumieć wykresy Lewisa. Wykresy Lewisa są czasami nazywane wykresami punktowymi. Są to proste diagramy, na których kropki reprezentują wolne i związane elektrony w zewnętrznej powłoce atomu. - Taki układ pozwala na rysowanie prostych diagramów, które odzwierciedlałyby wiązania między pierwiastkami w atomie lub cząsteczce np. kowalencyjnej.
 2 Dowiedz się, jaka jest reguła oktetu. Podczas konstruowania diagramów Lewisa używa się zasady oktetu, która mówi, że atom staje się stabilny, gdy ma dostęp do ośmiu elektronów w swojej zewnętrznej powłoce. Wyjątkiem jest wodór - uważa się go za stabilny, gdy w zewnętrznej powłoce znajdują się dwa elektrony.
2 Dowiedz się, jaka jest reguła oktetu. Podczas konstruowania diagramów Lewisa używa się zasady oktetu, która mówi, że atom staje się stabilny, gdy ma dostęp do ośmiu elektronów w swojej zewnętrznej powłoce. Wyjątkiem jest wodór - uważa się go za stabilny, gdy w zewnętrznej powłoce znajdują się dwa elektrony.  3 Narysuj diagram Lewisa. Symbol literowy elementu jest otoczony kropkami i jest diagramem Lewisa. Wyobraź sobie, że diagram to klatka filmu. Elektrony nie krążą wokół zewnętrznej powłoki pierwiastków - odbijają się w określonym czasie.
3 Narysuj diagram Lewisa. Symbol literowy elementu jest otoczony kropkami i jest diagramem Lewisa. Wyobraź sobie, że diagram to klatka filmu. Elektrony nie krążą wokół zewnętrznej powłoki pierwiastków - odbijają się w określonym czasie. - Schemat przedstawia stacjonarną masę elektronów, gdzie są one połączone z innym elementem, oraz informacje o wiązaniu (np. czy wiązania są podwojone i dzielone między kilka elektronów).
- Pomyśl o regule oktetu i wyobraź sobie symbol pierwiastka - na przykład C (węgiel). Narysuj po dwie kropki na wschodzie, zachodzie, północy i południu symbolu. Teraz narysuj symbol H (atom wodoru) po obu stronach każdej z kropek. Diagram pokazuje, że każdy atom węgla jest otoczony czterema atomami wodoru. Ich elektrony są związane kowalencyjnie, to znaczy w przypadku atomów węgla i wodoru jeden z elektronów jest związany z elektronem drugiego pierwiastka.
- Wzór cząsteczkowy takiego związku to CH4. Jest to gaz metanowy.
 4 Dowiedz się, jak elektrony wiążą pierwiastki. Diagramy Lewisa przedstawiają wiązania chemiczne w prostej formie.
4 Dowiedz się, jak elektrony wiążą pierwiastki. Diagramy Lewisa przedstawiają wiązania chemiczne w prostej formie. - Porozmawiaj na ten temat z nauczycielem i kolegami z klasy, jeśli nie rozumiesz, w jaki sposób elementy są połączone i co przedstawiają diagramy Lewisa.
 5 Dowiedz się, jak nazywają się połączenia. Chemia ma swoje własne zasady terminologiczne. Rodzaje reakcji, utrata lub zyskanie elektronów w powłoce zewnętrznej oraz stabilność lub niestabilność pierwiastków są częścią terminologii chemicznej.
5 Dowiedz się, jak nazywają się połączenia. Chemia ma swoje własne zasady terminologiczne. Rodzaje reakcji, utrata lub zyskanie elektronów w powłoce zewnętrznej oraz stabilność lub niestabilność pierwiastków są częścią terminologii chemicznej.  6 Potraktuj to poważnie. Wiele kursów chemii ma na to osobne rozdziały. Często nieznajomość terminologii oznacza oblanie egzaminu.
6 Potraktuj to poważnie. Wiele kursów chemii ma na to osobne rozdziały. Często nieznajomość terminologii oznacza oblanie egzaminu. - Jeśli to możliwe, zapoznaj się z terminologią przed zajęciami. Literaturę specjalistyczną można kupić w zwykłej księgarni lub w Internecie.
 7 Dowiedz się, co oznaczają liczby powyżej i poniżej linii. To bardzo ważna część nauki chemii.
7 Dowiedz się, co oznaczają liczby powyżej i poniżej linii. To bardzo ważna część nauki chemii. - Liczby nad linią widać w układzie okresowym pierwiastków. Reprezentują całkowity ładunek pierwiastka lub związku chemicznego. Zbadaj układ okresowy i elementy w pionowych rzędach, które mają te same numery indeksu.
- Liczby na dole wiersza służą do opisania ilości każdego pierwiastka, który wchodzi do związku. Jak wspomniano wcześniej, 2 we wzorze H2O wskazuje, że w cząsteczce wody znajdują się dwa atomy wodoru.
 8 Dowiedz się, jak atomy reagują ze sobą. W terminologii istnieją specjalne zasady, których należy przestrzegać przy nazywaniu produktów określonych typów reakcji.
8 Dowiedz się, jak atomy reagują ze sobą. W terminologii istnieją specjalne zasady, których należy przestrzegać przy nazywaniu produktów określonych typów reakcji. - Jedną z reakcji jest utlenianie-redukcja. Podczas reakcji następuje albo akwizycja, albo utrata elektronów.
- Elektrony są tracone podczas utleniania i nabywane podczas redukcji.
 9 Pamiętaj, że liczby na dole linii mogą wskazywać na formułę stabilnego ładunku związku. Naukowcy używają takich liczb do opisania ostatecznego wzoru cząsteczkowego związku, który oznacza również stabilny związek o ładunku obojętnym.
9 Pamiętaj, że liczby na dole linii mogą wskazywać na formułę stabilnego ładunku związku. Naukowcy używają takich liczb do opisania ostatecznego wzoru cząsteczkowego związku, który oznacza również stabilny związek o ładunku obojętnym. - Aby uzyskać ładunek neutralny, dodatnio naładowany jon, zwany kationem, musi być zrównoważony równym ładunkiem od jonu ujemnego, czyli anionu. Opłaty te są zapisane na dole wiersza.
- Na przykład w jonie magnezu jest +2 ładunek kationu, a w jonie azotu -3 ładunek anionu. +2 i -3 są wskazane na dole linii. Aby uzyskać ładunek neutralny, na każde 2 jednostki azotu potrzebne są 3 atomy magnezu.
- We wzorze jest to zapisane w następujący sposób: Mg3N2
 10 Naucz się rozpoznawać aniony i kationy na podstawie ich pozycji w układzie okresowym pierwiastków. Pierwiastki w tabeli znajdujące się w pierwszej kolumnie to metale alkaliczne i mają ładunek kationowy +1. Na przykład Na + i Li +.
10 Naucz się rozpoznawać aniony i kationy na podstawie ich pozycji w układzie okresowym pierwiastków. Pierwiastki w tabeli znajdujące się w pierwszej kolumnie to metale alkaliczne i mają ładunek kationowy +1. Na przykład Na + i Li +. - Metale ziem alkalicznych w drugiej kolumnie mają ładunek kationowy 2+, taki jak Mg2+ i Ba2+.
- Pierwiastki w siódmej kolumnie nazywane są halogenami i mają -1 ładunek anionów, takich jak Cl- i I-.
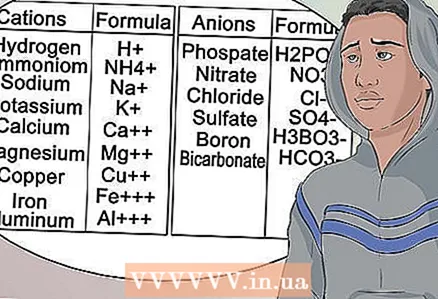 11 Naucz się rozpoznawać wspólne aniony i kationy. Aby zdać egzamin, naucz się całej terminologii związanej z grupami przedmiotów. Te liczby na dole wiersza nie zmieniają się.
11 Naucz się rozpoznawać wspólne aniony i kationy. Aby zdać egzamin, naucz się całej terminologii związanej z grupami przedmiotów. Te liczby na dole wiersza nie zmieniają się. - Innymi słowy, magnez to zawsze Mg z ładunkiem kationowym +2.
 12 Staraj się nie mylić z informacjami. Przejdą przez ciebie informacje o różnych rodzajach reakcji chemicznych, o wymianie elektronów, o zmianie ładunku pierwiastka lub jego składnika, a wszystko to będzie trudne do przyswojenia.
12 Staraj się nie mylić z informacjami. Przejdą przez ciebie informacje o różnych rodzajach reakcji chemicznych, o wymianie elektronów, o zmianie ładunku pierwiastka lub jego składnika, a wszystko to będzie trudne do przyswojenia. - Podziel trudne tematy na kawałki. Na przykład, jeśli nie rozumiesz reakcji utleniania lub zasady łączenia pierwiastków z ładunkami dodatnimi i ujemnymi, zacznij mówić wszystkie znane ci informacje, a zrozumiesz, że już dużo zrozumiałeś i zapamiętałeś.
 13 Regularnie rozmawiaj ze swoim nauczycielem. Zrób listę trudnych tematów i poproś nauczyciela o pomoc. Da ci to szansę na przyswojenie materiału, zanim grupa przejdzie do następnego tematu, co jeszcze bardziej zdezorientuje cię.
13 Regularnie rozmawiaj ze swoim nauczycielem. Zrób listę trudnych tematów i poproś nauczyciela o pomoc. Da ci to szansę na przyswojenie materiału, zanim grupa przejdzie do następnego tematu, co jeszcze bardziej zdezorientuje cię.  14 Wyobraź sobie, że chemia jest jak nauka nowego języka. Ważne jest, aby zrozumieć, że pisanie ładunków, liczba atomów w cząsteczce i wiązanie między cząsteczkami jest częścią języka chemii. Wszystko to odzwierciedla to, co dzieje się w przyrodzie na papierze.
14 Wyobraź sobie, że chemia jest jak nauka nowego języka. Ważne jest, aby zrozumieć, że pisanie ładunków, liczba atomów w cząsteczce i wiązanie między cząsteczkami jest częścią języka chemii. Wszystko to odzwierciedla to, co dzieje się w przyrodzie na papierze. - O wiele łatwiej byłoby to wszystko zrozumieć, gdyby wszystkie procesy można było obserwować na żywo. Ważne jest, abyś nie tylko zrozumiał zasady procesów, ale także język używany do zapisywania tych informacji.
- Jeśli masz trudności z nauką chemii, pamiętaj, że jesteś sam i nie poddawaj się. Porozmawiaj ze swoim instruktorem, grupą lub kimkolwiek, kto jest dobrze zorientowany w temacie. Tego wszystkiego można się nauczyć, ale byłoby lepiej, gdyby ktoś mógł ci wyjaśnić materiał, abyś wszystko zrozumiał.
Porady
- Nie zapomnij odpocząć. Przerwa w nauce pozwoli Ci wrócić do szkoły ze świeżym umysłem.
- Prześpij się w przeddzień egzaminu. Osoba śpiąca ma lepszą pamięć i koncentrację.
- Przeczytaj ponownie to, co już wiesz. Chemia to nauka zbudowana na badaniu jednego zjawiska i poszerzaniu wiedzy. Ważne jest, aby zachować w pamięci wszystko, czego się nauczyłeś, aby pytanie na egzaminie Cię nie zaskoczyło.
- Przygotuj się na zajęcia. Przeczytaj wszystkie materiały i odrób pracę domową. Jeśli coś przegapisz, będziesz coraz bardziej w tyle.
- Przydziel czas. Zwracaj większą uwagę na chemię, jeśli ten przedmiot nie jest dla ciebie dobry, ale nie poświęcaj mu całego czasu, ponieważ są inne przedmioty.