Autor:
Virginia Floyd
Data Utworzenia:
6 Sierpień 2021
Data Aktualizacji:
1 Lipiec 2024

Zawartość
- Kroki
- Metoda 1 z 3: Podstawy
- Metoda 2 z 3: Określanie rodzaju wiązania za pomocą elektroujemności
- Metoda 3 z 3: Obliczanie elektroujemności Mullikena
- Porady
W chemii elektroujemność to zdolność atomów do przyciągania do nich elektronów z innych atomów. Atom o wysokiej elektroujemności silnie przyciąga elektrony, a atom o niskiej elektroujemności słabo przyciąga elektrony. Wartości elektroujemności służą do przewidywania zachowania różnych atomów w związkach chemicznych.
Kroki
Metoda 1 z 3: Podstawy
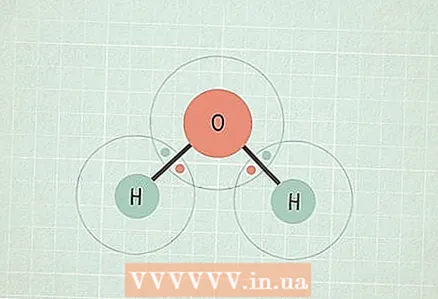 1 Wiązania chemiczne. Takie wiązania powstają, gdy elektrony w atomach oddziałują ze sobą, to znaczy, że dwa elektrony (po jednym z każdego atomu) stają się wspólne.
1 Wiązania chemiczne. Takie wiązania powstają, gdy elektrony w atomach oddziałują ze sobą, to znaczy, że dwa elektrony (po jednym z każdego atomu) stają się wspólne. - Opis przyczyn oddziaływania elektronów w atomach wykracza poza zakres tego artykułu.Więcej informacji na ten temat znajdziesz na przykład w tym artykule.
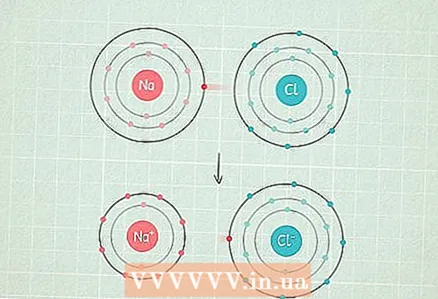 2 Wpływ elektroujemności. Kiedy dwa atomy przyciągają elektrony, siła przyciągania nie jest taka sama. Atom o wyższej elektroujemności silniej przyciąga dwa elektrony. Atom o bardzo wysokiej elektroujemności przyciąga elektrony z taką siłą, że nie mówimy już o elektronach wspólnych.
2 Wpływ elektroujemności. Kiedy dwa atomy przyciągają elektrony, siła przyciągania nie jest taka sama. Atom o wyższej elektroujemności silniej przyciąga dwa elektrony. Atom o bardzo wysokiej elektroujemności przyciąga elektrony z taką siłą, że nie mówimy już o elektronach wspólnych. - Na przykład w cząsteczce NaCl (chlorek sodu, sól kuchenna) atom chloru ma dość wysoką elektroujemność, a atom sodu jest raczej niski. Więc elektrony są przyciągane do atomu chloru oraz odpychają atomy sodu.
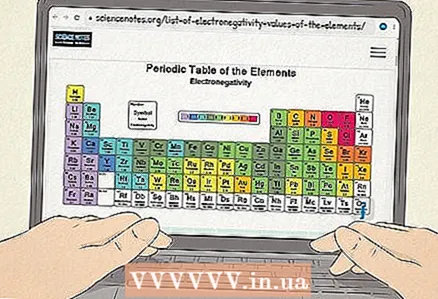 3 Tabela elektroujemności. Ta tabela zawiera pierwiastki chemiczne ułożone w taki sam sposób jak w układzie okresowym, ale dla każdego pierwiastka podana jest elektroujemność jego atomów. Taką tabelę można znaleźć w podręcznikach do chemii, materiałach referencyjnych oraz w Internecie.
3 Tabela elektroujemności. Ta tabela zawiera pierwiastki chemiczne ułożone w taki sam sposób jak w układzie okresowym, ale dla każdego pierwiastka podana jest elektroujemność jego atomów. Taką tabelę można znaleźć w podręcznikach do chemii, materiałach referencyjnych oraz w Internecie. - Znajdziesz tutaj doskonały stół elektroujemności. Zauważ, że używa skali elektroujemności Paulinga, która jest najczęstsza. Istnieją jednak inne sposoby obliczania elektroujemności, z których jeden zostanie omówiony poniżej.
 4 Trendy elektroujemności. Jeśli nie masz pod ręką tabeli elektroujemności, możesz oszacować elektroujemność atomu na podstawie położenia pierwiastka w układzie okresowym.
4 Trendy elektroujemności. Jeśli nie masz pod ręką tabeli elektroujemności, możesz oszacować elektroujemność atomu na podstawie położenia pierwiastka w układzie okresowym. - Jak w prawo element znajduje się, jeszcze elektroujemność jego atomu.
- Jak wyższy element znajduje się, jeszcze elektroujemność jego atomu.
- Zatem atomy pierwiastków znajdujących się w prawym górnym rogu układu okresowego mają najwyższe elektroujemności, a atomy pierwiastków znajdujących się w lewym dolnym rogu mają najniższe.
- W naszym przykładzie NaCl możemy powiedzieć, że chlor ma wyższą elektroujemność niż sód, ponieważ chlor znajduje się na prawo od sodu.
Metoda 2 z 3: Określanie rodzaju wiązania za pomocą elektroujemności
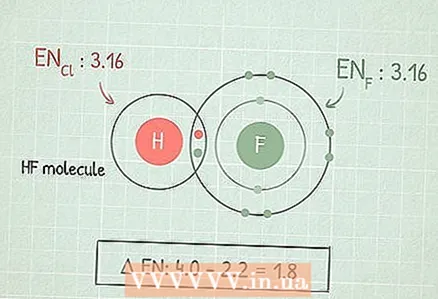 1 Oblicz różnicę między elektroujemnościami dwóch atomów, aby zrozumieć charakterystykę wiązania między nimi. Aby to zrobić, odejmij mniejszą elektroujemność od większej.
1 Oblicz różnicę między elektroujemnościami dwóch atomów, aby zrozumieć charakterystykę wiązania między nimi. Aby to zrobić, odejmij mniejszą elektroujemność od większej. - Rozważmy na przykład cząsteczkę HF. Odejmij elektroujemność wodoru (2,1) od elektroujemności fluoru (4,0): 4,0 - 2,1 = 1,9.
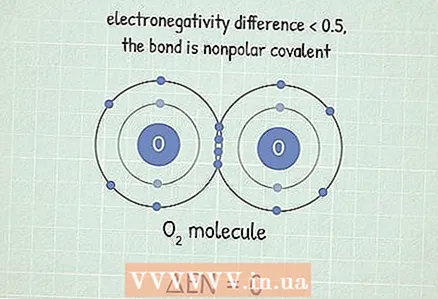 2 Jeśli różnica jest mniejsza niż 0,5, to wiązanie jest kowalencyjne niepolarne, w którym elektrony są przyciągane z prawie taką samą siłą. Takie wiązania powstają między dwoma identycznymi atomami. Połączenia niepolarne są na ogół bardzo trudne do zerwania. Dzieje się tak, ponieważ atomy dzielą elektrony, co sprawia, że ich wiązanie jest stabilne. Zniszczenie go wymaga dużo energii.
2 Jeśli różnica jest mniejsza niż 0,5, to wiązanie jest kowalencyjne niepolarne, w którym elektrony są przyciągane z prawie taką samą siłą. Takie wiązania powstają między dwoma identycznymi atomami. Połączenia niepolarne są na ogół bardzo trudne do zerwania. Dzieje się tak, ponieważ atomy dzielą elektrony, co sprawia, że ich wiązanie jest stabilne. Zniszczenie go wymaga dużo energii. - Na przykład cząsteczka O2 ma tego typu połączenie. Ponieważ dwa atomy tlenu mają taką samą elektroujemność, różnica między nimi wynosi 0.
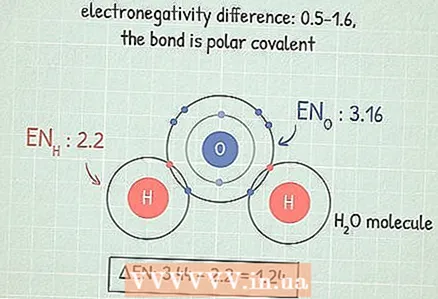 3 Jeżeli różnica mieści się w zakresie 0,5 – 1,6, to wiązanie jest polarne kowalencyjnie. W tym przypadku jeden z dwóch atomów silniej przyciąga elektrony i dlatego uzyskuje częściowy ładunek ujemny, a drugi częściowy ładunek dodatni. Ta nierównowaga ładunku pozwala cząsteczce uczestniczyć w pewnych reakcjach.
3 Jeżeli różnica mieści się w zakresie 0,5 – 1,6, to wiązanie jest polarne kowalencyjnie. W tym przypadku jeden z dwóch atomów silniej przyciąga elektrony i dlatego uzyskuje częściowy ładunek ujemny, a drugi częściowy ładunek dodatni. Ta nierównowaga ładunku pozwala cząsteczce uczestniczyć w pewnych reakcjach. - Na przykład cząsteczka H2O (woda) ma ten rodzaj wiązania. Atom O jest bardziej elektroujemny niż dwa atomy H, więc tlen silniej przyciąga elektrony i uzyskuje częściowy ładunek ujemny, a wodór częściowy ładunek dodatni.
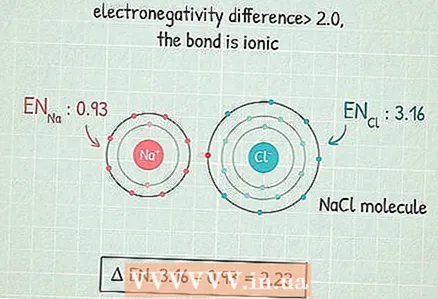 4 Jeśli różnica jest większa niż 2,0, to wiązanie jest jonowe. Jest to wiązanie, w którym wspólna para elektronów przechodzi głównie do atomu o wyższej elektroujemności, który uzyskuje ładunek ujemny, a atom o niższej elektroujemności uzyskuje ładunek dodatni. Cząsteczki z takimi wiązaniami dobrze reagują z innymi atomami, a nawet mogą zostać zniszczone przez atomy polarne.
4 Jeśli różnica jest większa niż 2,0, to wiązanie jest jonowe. Jest to wiązanie, w którym wspólna para elektronów przechodzi głównie do atomu o wyższej elektroujemności, który uzyskuje ładunek ujemny, a atom o niższej elektroujemności uzyskuje ładunek dodatni. Cząsteczki z takimi wiązaniami dobrze reagują z innymi atomami, a nawet mogą zostać zniszczone przez atomy polarne. - Na przykład cząsteczka NaCl (chlorek sodu) ma ten rodzaj wiązania.Atom chloru jest tak elektroujemny, że przyciąga do siebie oba elektrony i uzyskuje ładunek ujemny, a atom sodu uzyskuje ładunek dodatni.
- NaCl może zostać zniszczony przez cząsteczkę polarną, taką jak H2O (woda). W cząsteczce wody strona wodorowa cząsteczki jest dodatnia, a tlenowa ujemna. Jeśli zmieszasz sól z wodą, cząsteczki wody rozbijają cząsteczki soli, powodując jej rozpuszczenie.
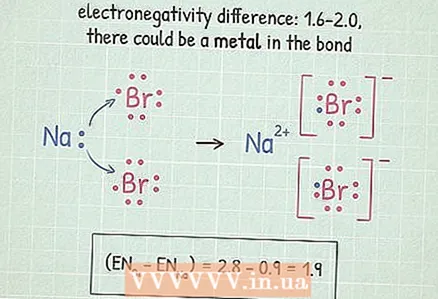 5 Jeśli różnica wynosi od 1,6 do 2,0, sprawdź metal. Jeśli atom metalu jest obecny w cząsteczce, to wiązanie jest jonowe. Jeśli w cząsteczce nie ma atomów metalu, wiązanie jest kowalencyjne polarne.
5 Jeśli różnica wynosi od 1,6 do 2,0, sprawdź metal. Jeśli atom metalu jest obecny w cząsteczce, to wiązanie jest jonowe. Jeśli w cząsteczce nie ma atomów metalu, wiązanie jest kowalencyjne polarne. - Metale znajdują się po lewej i pośrodku układu okresowego. W tej tabeli podświetlone są metale.
- W naszym przykładzie HF różnica między elektroujemnościami mieści się w tym zakresie. Ponieważ H i F nie są metalami, wiązanie kowalencyjny polarny.
Metoda 3 z 3: Obliczanie elektroujemności Mullikena
 1 Znajdź pierwszą energię jonizacji atomu. Skala elektroujemności Mullikena różni się nieco od wspomnianej powyżej skali Paulinga. Pierwsza energia jonizacji jest wymagana do usunięcia jednego atomu z elektronu.
1 Znajdź pierwszą energię jonizacji atomu. Skala elektroujemności Mullikena różni się nieco od wspomnianej powyżej skali Paulinga. Pierwsza energia jonizacji jest wymagana do usunięcia jednego atomu z elektronu. - Znaczenie takiej energii można znaleźć w książkach do chemii lub w sieci, na przykład tutaj.
- Jako przykład znajdźmy elektroujemność litu (Li). Jego pierwsza energia jonizacji to 520 kJ/mol.
 2 Znajdź energię powinowactwa dla elektronu. Jest to energia uwalniana w procesie przyłączania elektronu do atomu. Znaczenie takiej energii można znaleźć w książkach do chemii lub w sieci, na przykład tutaj.
2 Znajdź energię powinowactwa dla elektronu. Jest to energia uwalniana w procesie przyłączania elektronu do atomu. Znaczenie takiej energii można znaleźć w książkach do chemii lub w sieci, na przykład tutaj. - Energia powinowactwa elektronowego litu wynosi 60 kJ/mol.
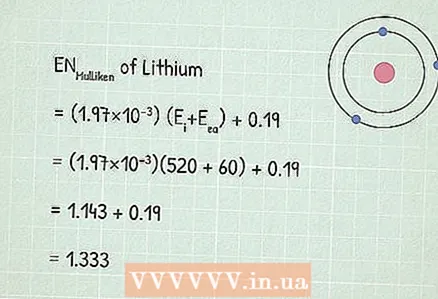 3 Użyj równania elektroujemności Mullikena:RUMulliken = (1,97 × 10) (Ei+ Etak) + 0,19.
3 Użyj równania elektroujemności Mullikena:RUMulliken = (1,97 × 10) (Ei+ Etak) + 0,19. - W naszym przykładzie:
- RUMulliken = (1,97 × 10) (Ei+ Etak) + 0,19
- RUMulliken = (1,97×10)(520 + 60) + 0,19
- RUMulliken = 1,143 + 0,19 = 1,333
- W naszym przykładzie:
Porady
- Oprócz skal Paulinga i Mullikena istnieją skale elektroujemności według Allreda-Rochowa, Sandersona, Allena. Wszystkie mają własne wzory do obliczania elektroujemności (niektóre z nich są dość skomplikowane).
- Elektroujemność nie ma jednostek miary.