Autor:
Christy White
Data Utworzenia:
8 Móc 2021
Data Aktualizacji:
1 Lipiec 2024

Zawartość
- Do kroku
- Metoda 1 z 3: Część pierwsza: Zrozumienie powłok elektronowych
- Metoda 2 z 3: Część druga: Znajdowanie elektronów walencyjnych w metalach, z wyjątkiem metali przejściowych
- Metoda 3 z 3: Część trzecia: Znajdowanie elektronów walencyjnych w metalach przejściowych
- Porady
- Potrzeby
Elektrony walencyjne znajdują się w zewnętrznej powłoce elementu. Liczba elektronów walencyjnych w atomie określa rodzaj wiązania chemicznego, jakie ten pierwiastek może utworzyć. Najlepszym sposobem ustalenia liczby elektronów walencyjnych jest użycie układu okresowego pierwiastków.
Do kroku
Metoda 1 z 3: Część pierwsza: Zrozumienie powłok elektronowych
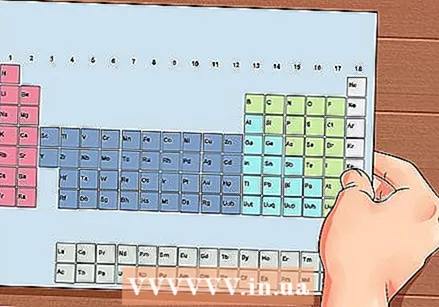 Układ okresowy pierwiastków. Jest to tabela z kodami kolorów, w której w każdej komórce wyświetlany jest element z liczbą atomową i od 1 do 3 liter jako symbol.
Układ okresowy pierwiastków. Jest to tabela z kodami kolorów, w której w każdej komórce wyświetlany jest element z liczbą atomową i od 1 do 3 liter jako symbol. 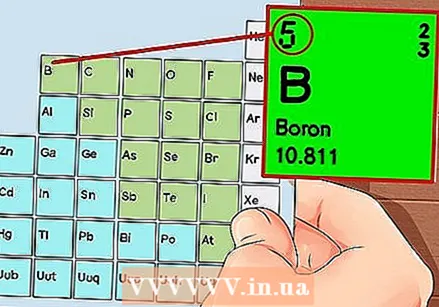 Znajdź liczbę atomową pierwiastka. Liczba atomowa znajduje się powyżej lub obok symbolu elementu. Na przykład: Bor (B) ma liczbę atomową 5, co oznacza, że ma 5 protonów i 5 elektronów.
Znajdź liczbę atomową pierwiastka. Liczba atomowa znajduje się powyżej lub obok symbolu elementu. Na przykład: Bor (B) ma liczbę atomową 5, co oznacza, że ma 5 protonów i 5 elektronów. 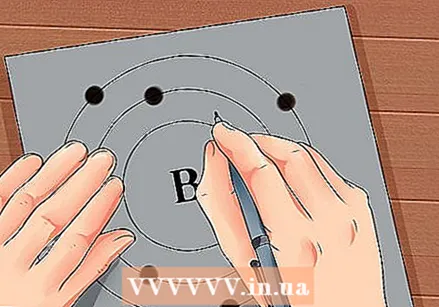 Narysuj prostą reprezentację atomu i umieść elektrony na orbicie wokół jądra. Te prace są również nazywane muszlami lub poziomami energii. Maksymalna liczba elektronów, które mogą znajdować się w tej samej powłoce, jest stała, a powłoki są wypełniane od wewnętrznej do zewnętrznej orbity.
Narysuj prostą reprezentację atomu i umieść elektrony na orbicie wokół jądra. Te prace są również nazywane muszlami lub poziomami energii. Maksymalna liczba elektronów, które mogą znajdować się w tej samej powłoce, jest stała, a powłoki są wypełniane od wewnętrznej do zewnętrznej orbity. - Powłoka K (wewnętrzna): maksymalnie 2 elektrony.
- L Shell: maksymalnie 8 elektronów.
- Powłoka M: maksymalnie 18 elektronów.
- Powłoka N: maksymalnie 32 elektrony.
- O Shell: maksymalnie 50 elektronów.
- Powłoka P (zewnętrzna): maksymalnie 72 elektrony.
 Znajdź liczbę elektronów w powłoce zewnętrznej. To są elektrony walencyjne.
Znajdź liczbę elektronów w powłoce zewnętrznej. To są elektrony walencyjne. - Gdy powłoka walencyjna jest pełna, element jest stabilny.
- Jeśli powłoka walencyjna nie jest pełna, to pierwiastek jest reaktywny, co oznacza, że może wiązać się chemicznie z atomem innego pierwiastka. Każdy atom dzieli swoje elektrony walencyjne, próbując napełnić powłokę walencyjną.
Metoda 2 z 3: Część druga: Znajdowanie elektronów walencyjnych w metalach, z wyjątkiem metali przejściowych
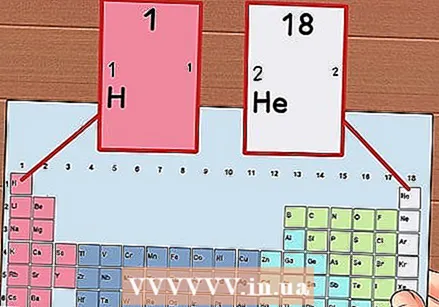 Ponumeruj każdą kolumnę układu okresowego od 1 do 18. Wodór (H) znajduje się na górze kolumny 1, a hel (He) na szczycie kolumny 18. Są to różne grupy pierwiastków.
Ponumeruj każdą kolumnę układu okresowego od 1 do 18. Wodór (H) znajduje się na górze kolumny 1, a hel (He) na szczycie kolumny 18. Są to różne grupy pierwiastków. 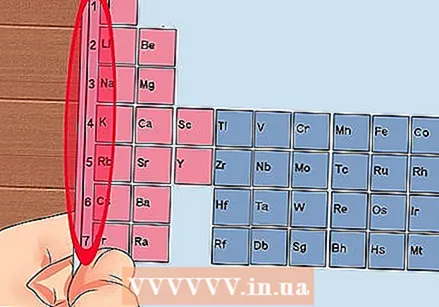 Nadaj każdemu wierszowi liczbę od 1 do 7. To są okresy pierwiastków i odpowiadają one liczbie powłok lub poziomach energetycznych atomu.
Nadaj każdemu wierszowi liczbę od 1 do 7. To są okresy pierwiastków i odpowiadają one liczbie powłok lub poziomach energetycznych atomu. - Wodór (H) i hel (He) mają po 1 skorupie, podczas gdy Francium (Fr) ma 7.
- Lantanowce i aktynowce są pogrupowane i wymienione poniżej głównej tabeli. Wszystkie lantanowce należą do okresu 6, grupy 3, a wszystkie aktynowce należą do okresu 7, grupy 3.
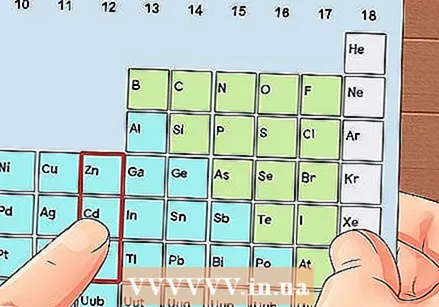 Zlokalizuj element, który nie jest metalem przejściowym. Metale przejściowe znajdują się w grupach od 3 do 12. Numery grup innych metali wskazują liczbę elektronów walencyjnych.
Zlokalizuj element, który nie jest metalem przejściowym. Metale przejściowe znajdują się w grupach od 3 do 12. Numery grup innych metali wskazują liczbę elektronów walencyjnych. - Grupa 1: 1 elektron walencyjny
- Grupa 2: 2 elektrony walencyjne
- Grupa 13: 3 elektrony walencyjne
- Grupa 14: 4 elektrony walencyjne
- Grupa 15: 5 elektronów walencyjnych
- Grupa 16: 6 elektronów walencyjnych
- Grupa 17: 7 elektronów walencyjnych
- Grupa 18: 8 elektronów walencyjnych - z wyjątkiem helu, który ma 2
Metoda 3 z 3: Część trzecia: Znajdowanie elektronów walencyjnych w metalach przejściowych
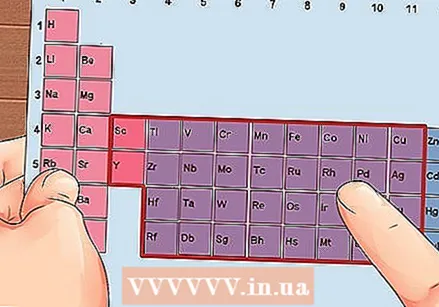 Znajdź pierwiastek z grup 3 do 12, metale przejściowe.
Znajdź pierwiastek z grup 3 do 12, metale przejściowe. Określ liczbę elektronów walencyjnych na podstawie numeru grupy. Te numery grup odpowiadają możliwej liczbie elektronów walencyjnych.
Określ liczbę elektronów walencyjnych na podstawie numeru grupy. Te numery grup odpowiadają możliwej liczbie elektronów walencyjnych. - Grupa 3: 3 elektrony walencyjne
- Grupa 4: 2 do 4 elektronów walencyjnych
- Grupa 5: 2 do 5 elektronów walencyjnych
- Grupa 6: 2 do 6 elektronów walencyjnych
- Grupa 7: 2 do 7 elektronów walencyjnych
- Grupa 8: 2 lub 3 elektrony walencyjne
- Grupa 9: 2 lub 3 elektrony walencyjne
- Grupa 10: 2 lub 3 elektrony walencyjne
- Grupa 11: 1 lub 2 elektrony walencyjne
- Grupa 12: 2 elektrony walencyjne
Porady
- Metale przejściowe mogą mieć skorupy walencyjne, które nie są całkowicie pełne. Określenie dokładnej liczby elektronów walencyjnych w metalach przejściowych wymaga pewnych zasad teorii kwantów, które wykraczają poza zakres tego artykułu.
Potrzeby
- Układ okresowy pierwiastków
- Ołówek
- Papier